ミルセラ®による移植後貧血の正常化と天然型ビタミンD3の補充が移植腎機能に及ぼす影響を検討するランダム化比較試験:CANDLE-KIT Trial
研究の目的
腎移植は、末期腎不全の患者さんの生命予後と生活の質を大きく向上できる、非常に優れた治療法です。現在は免疫抑制剤の発達によって、かなり長期に生着することができるようになりましたが、それでも年月とともに徐々に腎機能が低下していくことが少なくありません。この移植腎の機能低下を抑制するために様々な試みが行われていますが、赤血球造血刺激因子製剤(ESA)による貧血治療と天然型ビタミンDが有効ではないかと期待されています。
腎移植後には、様々な理由から貧血を合併することが少なくありません(移植後貧血)。この貧血を、赤血球造血刺激因子製剤を用いて正常範囲まで改善することで、腎機能の低下を抑制できることがフランスの研究で示されています。また、ビタミンDは尿蛋白や炎症を抑制する作用、免疫を整える作用を持つ可能性が知られています。腎移植後はビタミンDが欠乏しやすいことが知られており、天然型ビタミンDの投与によって、予後が改善されることが期待されます。さらに、抗炎症作用によって目標ヘモグロビン値を達成するために必要なESAの投与量が少なくなる可能性も指摘されており、これによってESAの副作用や必要な医療費が抑制できる可能性があります。
しかしながら、良いことばかりではありません。赤血球造血刺激因子製剤は、保存期腎不全でも同様の腎機能低下抑制効果が期待され多くの研究が行われましたが、有効性は明らかではありませんでした。一方で、高血圧などの副作用が生じる可能性があります。また、この薬剤は非常に高価であり、過度の使用は医療費の高騰を招いてしまうことが懸念されます。一方、一般的に天然型ビタミンDは非常に安全なサプリメントと考えられていますが、腎移植を受けた方によっては血液中のカルシウムイオン濃度が高くなりすぎるかもしれません。この場合、筋力低下,便秘,食欲不振,悪心・嘔吐,多尿,多飲などの症状を呈し、移植腎に障害を来す可能性があります。
これらの薬剤が、諸外国と比べて人種や医療環境の異なる日本において、どの程度有効で、本当に安全に投与できるのかを科学的に検証する必要があります。私達は、この研究から得られた知見を世界の腎移植医療の向上に役立て、将来の患者さんに より良い治療を提供したいと考えています。
研究の方法
この研究は、移植後1年以上経過し、かつ 貧血を合併している腎移植患者さんを対象としています。
実施予定期間と目標症例数
実施予定期間は、2013年2月から2019年3月末までとなっています。患者さん個人に関しては、者さん個人に関しては、参加登録から試験終了までは2年間となっていますが、終了後も1年間の観察を行います。また、計246人の患者さんに参加していただく予定です。
介入の割り付け
この研究では、① 赤血球造血刺激因子製剤(中外製薬社 ミルセラ®)による貧血の治療目標ヘモグロビン値を(A)正常化(12.5 g/dL以上13.5
g/dL未満)とする場合と(B)9.5 g/dL以上10.5g/dL未満とする場合の効果を比較すると同時に、 ② 天然型ビタミンDサプリメントを(C)1日あたり1,000単位投与する場合と(D)投与しない場合
を比較するために、4つのグループに分けて治療を行います。どのグループになるかは、くじを引くような方法で決められ、それぞれの確率は4分の1です。どれに割り付けられるかを患者さんも担当医師も選択することができません。この方法を
無作為割付(ランダム化)といいます。

Ⅰ群 目標Hb値 12.5 g/dL以上13.5 g/dL未満 かつ 天然型ビタミンD3 1,000単位/日
Ⅱ群 目標Hb値 9.5 g/dL以上10.5 g/dL未満 かつ 天然型ビタミンD3 1,000単位/日
Ⅲ群 目標Hb値 12.5 g/dL以上13.5 g/dL未満 かつ 天然型ビタミンD3 投与無し
Ⅳ群 目標Hb値 9.5 g/dL以上10.5 g/dL未満 かつ 天然型ビタミンD3 投与無し
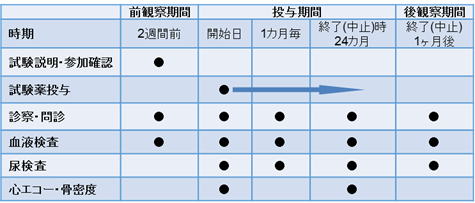
臨床試験スケジュール
・ 治療開始前に血液検査、尿検査を行います。
・ 天然型ビタミンDを内服する場合、1日1回1錠(1,000単位)を内服してください。
・ 移植後貧血に関しては、血液検査の結果を見て、担当医が必要に応じたミルセラ®の注射を行います。
・ 基本的に1ヶ月毎に 来院していただきます。受診時には血液検査と尿検査を行います。
・ 開始時・1ヶ月後・6ヶ月後・1年後・2年後の血液検査を行う時に、通常より6cc多めに採取いたします。
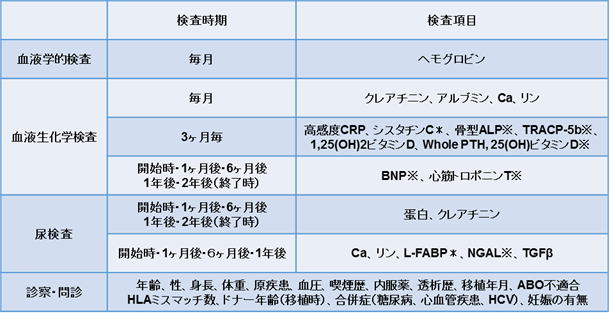
※ 保険適応外の項目(骨型ALP、TRACP-5、25(OH)ビタミンD、BNP、心筋トロポニンT、尿中NGAL、尿TGFβ)は、 研究費で測定します。
* シスタチンCと尿中L-FABPに関しては、1か月後の測定は行いません。
可能性のある副作用
副作用には個人差があり、必ず起こるというわけではありません。ただし、どんな薬でも副作用がおこる可能性はあるので、何か異常があれば お知らせ下さい。
ミルセラ®
起こりやすい副作用
・ 1%以上 内シャントの狭窄や閉塞、高血圧、好酸球数の増加
頻度はかなりまれですが、起こると重大な副作用
・ 0.2% 脳出血、心筋梗塞、高血圧性脳症(※1)
・ 頻度不明 脳梗塞、肺梗塞、赤芽球癆(※2)、肝障害、アレルギー、ショック、アナフィラキシー(※3)
※1 著しい血圧の上昇、頭痛、悪心、嘔吐、意識障害など
※2 赤血球造血刺激因子製剤に対するアレルギーによる重篤な貧血
※3 じんましん、血圧低下、口唇の腫れ、呼吸困難などの症状
天然型ビタミンD
起こりうる副作用
・ 頻度不明 高カルシウム血症(筋力低下, 便秘,悪心・嘔吐,多尿,多飲,情緒不安定など)
健康被害が生じた場合
本研究は細心の注意をもって行われます。もし、この研究期間中に何らかの健康被害が生じた場合、補償はありませんが、医師が最善を尽くして適切な処置と治療を行います。費用は通常の診療と同様に健康保険による患者さんの自己負担となります。医薬品の副作用によって入院が必要な程度の疾病や障害などの健康被害が生じた場合には、医薬品副作用被害救済制度に基づき医療費等の給付を請求できる場合があります。
研究計画及び研究成果の開示
本研究の計画や その成果に関する情報は、当講座のホームページに随時公開されます。各参加施設のホームページからも、リンクを通して閲覧が可能です。さらに詳しい内容を知りたい場合は、他の患者さんの個人情報保護やこの研究の独創性の確保に支障がない範囲内で、ご説明致します。患者さんが同意されれば、御家族等(親権者、配偶者、兄弟姉妹、成人の子、後見人など)を交えてお話しすることも可能です。
知的財産権の帰属
なお本研究の成果により、何らかの特許権等や それによる経済的利益が生み出される可能性がありますが、全ての権利は研究機関、民間企業を含む共同研究機関
および研究遂行者などに帰属します。
研究への参加にともなう費用について
この研究では、貧血治療に関して2つのグループに分けて治療を行いますが、目標ヘモグロビン値を12.5 g/dL以上13.5 g/dL未満とするグループでは、薬剤費が高額となる可能性があります。研究期間中の検査や治療のうち、保険適応内のものは 通常診療と同じように扱われますので、どのような社会福祉制度(身体障害者手帳など)を受けているかによって、大きく自己負担額が変わります。どちらのグループになるかは選べませんので、担当医にご相談のうえ、よく考えて研究への参加を決めてください。なお、保険適応外の天然型ビタミンDや一部の研究目的の特殊検査(血中ビタミンD濃度や尿中腎障害マーカーなど)は、研究費より支払われます。また、謝礼や交通費などの支給はありません。
参加・不参加や 同意の撤回に 制約はありません
この研究への参加は、患者さんの自由な意思で決めてください。たとえお断りになっても今後の治療において不利益を受けることはありません。またこの研究への参加に同意した後にも、いつでも同意を撤回することができます。この場合も、診療にあたって不利益を受けることはなく、患者さんに合った治療法を行っていきます。同意の撤回を希望される場合は、遠慮なく担当医師にお伝えください。該当する患者さんに関わる研究結果を破棄し、それ以降は
得られた情報を研究目的に用いないようにすることが可能です。ただし、すでに研究結果が公表されていた場合は、これを破棄することはできません。
個人情報の保護
この研究で得られた情報を取りまとめるために、当院以外の機関にも患者さんの生年月日や検査結果、内服薬などの情報を提供することがあります。ただし、その際には個人を特定できる情報は記載しません。取りまとめられた情報を医学雑誌などに発表する場合も、個人が特定できないように配慮されます。また、この研究が適切に行われているかを確認するために関係者がカルテなどを見ることがありますが、その場合もプライバシーは守られます。
知的財産権の帰属
なお本研究の成果により、何らかの特許権等や それによる経済的利益が生み出される可能性がありますが、全ての権利は研究機関、民間企業を含む共同研究機関
および研究遂行者などに帰属します。
資金源及び関連組織との関わり
この研究は、日本学術振興会の科学研究費助成と日本腎臓財団の腎不全病態研究助成から提供された資金で実施します。他にも、大阪大学大学院 医学系研究科
腎疾患統合医療寄附講座の研究費で、研究に必要な経費が賄われます。この講座は、中外製薬(株)および バクスター(株)から 研究資金の寄付を受けており、本研究に際しては中外製薬(株)から追加の資金提供を受けています。また、協和メディックス(株)の協力で血清25-ヒドロキシビタミンDを、DSファーマバイオメディカル(株)の協力でTRACP-5bを測定します。ただし、担当医師が個人的に利益を得ることはなく、研究は公正に行われます。
資料及び試料の利用と保存
この研究で得られたデータ、および血液や尿は、研究終了後も 大阪大学大学院医学系研究科 老年・腎臓内科で保管され、他の研究に利用する可能性があります。これらの2次利用については、別紙「包括同意説明文書」をよく読んだ上で、ご協力いただける場合は、包括同意書にご署名をお願いします。お断りになる場合は、研究終了後、当院の規定に従って廃棄します。
研究組織
この試験は、大阪大学大学院 医学系研究科 腎疾患統合医療寄附講座が主体となって実施します。以下に示す施設が参加しています。
北海道大学病院 市立札幌病院 秋田大学医学部附属病院 JCHO仙台病院 自治医科大学附属病院 国立水戸医療センター 千葉東病院 北里大学病院 虎の門病院分院 聖マリアンナ医科大学附属病院 東京女子医科大学病院 東邦大学医療センター大森病院 社会保険中京病院 サンシャインM&Dクリニック 岐阜大学医学部附属病院 名古屋第二赤十字病院 藤田保健衛生大学 奈良県立医科大学付属病院 大阪大学医学部附属病院 大阪市立大学医学部附属病院 大阪府立急性期医療センター 兵庫県立西宮病院 蒼龍会井上病院 大阪みなと中央病院(旧:大阪船員保険病院) 住友病院 愛仁会高槻病院 日本赤十字社和歌山医療センター 香川大学医学部附属病院 高知医療センター 岡山大学病院 岡山医療センター 九州大学病院 原三信病院 熊本赤十字病院 豊見城中央病院 新潟大学医歯学総合病院
・ 主任研究者(試験全体を統括する研究者)
椿原美治(大阪大学大学院 医学系研究科 腎疾患統合医療学寄附講座)
・ データセンター(データ管理を行う施設)
大阪大学大学院 医学系研究科 先端移植基盤医療講座 (責任者:市丸直嗣)
お問い合わせ先
本研究に関し、疑問、苦情などある際には、下記研究事務局までご連絡ください。
大阪大学大学院 医学系研究科 腎疾患統合医療学
事務局責任者:濱野高行(寄附講座准教授)
住所:大阪府吹田市山田丘2-2
電話番号:06-6879-3857
バナースペース
大阪大学大学院医学系研究科
腎疾患統合医療学
Department of Comprehensive Kidney Disease Research,
Osaka University Graduate School of Medicine
〒565-0871
大阪府吹田市山田丘2-2
バイオ棟6階 E60-01
TEL 06-6879-3747
FAX 06-6879-3746
2-2, Yamada-oka, Suita, Osaka, 565-0871, Japan
TEL +81-6-6879-3747
FAX +81-6-6879-3746
・大阪大学大学院医学系研究科
・大阪大学医学部附属病院
・大阪大学 腎臓内科
・大阪大学 老年・総合内科学